3D 프린트 맞춤형의료기기 인증,허가 주요내용
안녕하세요!
오늘은 3D 프린트 맞춤형 의료기기의 인증, 허가에 필요한 주요 내용에 대해 알아보겠습니다.

사용자 맞춤형 의료기기의 인증도 어려운데, 여기에 3D 프린트가 들어간다면 필요한 제출자료가 더 많아지게 됩니다. 하지만 요즘 3D 프린트 의료기기 시장이 활성화되고 있어서 꼭 알아야 하는 중요한 내용이 아닐까 생각합니다.
주요 내용으로 기술문서 작성에 필요한 내용과 기술문서심사를 위한 제출자료에 대해 알아보겠습니다. 각 품목 군의 성능, 안정성을 위한 자료에 더불어 3D 프린팅 제품이기 때문에 추가되는 자료가 있기 때문에 꼭 확인하셔야 하는 내용입니다.
기술문서 작성 요령
명칭

명칭은 환자에 따라 치수가 변경된다면 제조될 수 있는 부분을 구분하여 모델명을 기재하게 됩니다.
하지만 저의 경험으로는 변경되는 치수가 명칭에 꼭 반영되진 않아도 괜찮았습니다. 단, 각 사용자가 구분될 수 있도록 LOT No 등의 추적성은 유지되어야 합니다.
모양 및 구조
작용 원리

작용 원리에는 3D 프린트 관련 특징이 기재되어야 합니다.
대표 기술, 원리, 장점 외에도 재료의 형태(파우더, 액체, 등), 적층 두께, 출력, 경화시간 등의 사양이 기재될 수도 있습니다.
외형
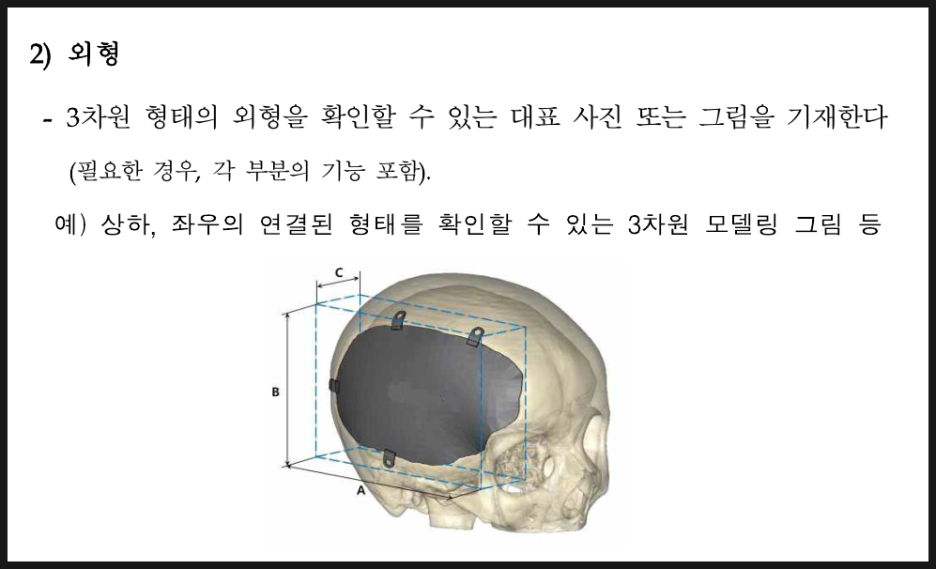
외형은 실제 완제품의 사진을 넣으면 되고, 때론 3D 프린트되기 전의 재료의 형상이 요구되기도 합니다.
치수 및 중량
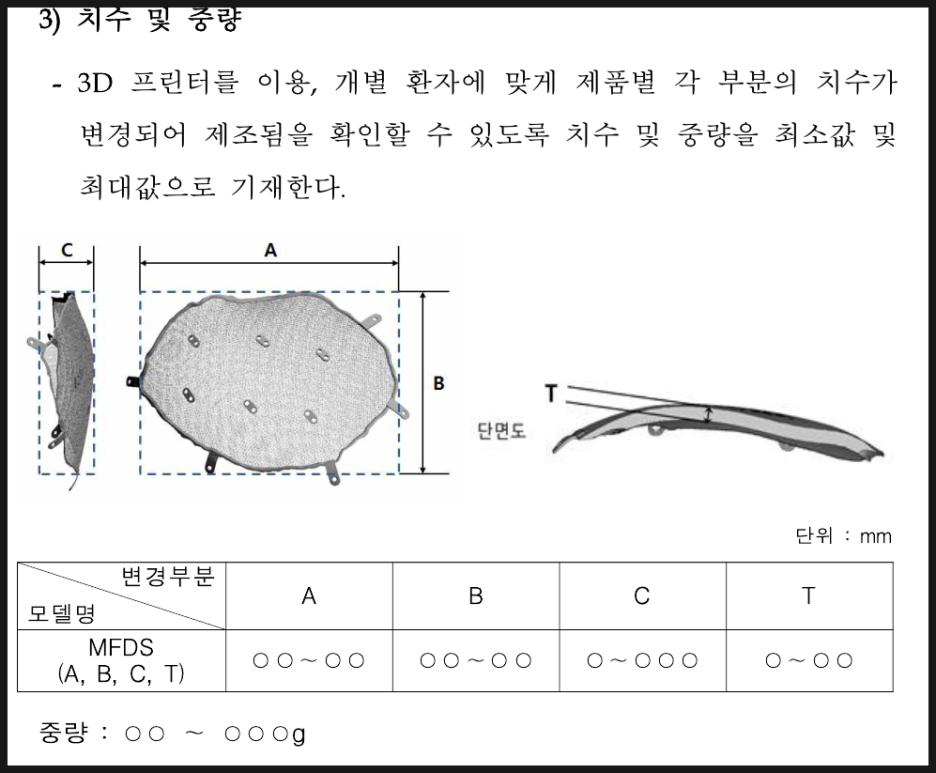
치수는 환자에 따라 치수가 변경된다면 변경되는 범위에 따라 기재됩니다.
사용목적

사용목적에는 3D프린터에 관한 사항이 기재되어야 합니다.
예를 들어,"3D 프린트를 사용하여 제조되는 환자 맞춤형 의료기기로 ~" 등의 문장이 들어가야 합니다.
사용방법

사용 전 준비사항에는 "사용 전에 의사 처방 유무를 확인하고, 처방과 관련된 제품에 적용된 환자 병변 데이터 일치 여부 등의 확인이 필요하다." 문장이 추가되어야 합니다.
기술문서 심사 시 제출자료
기술문서 심사 시 제출자료로는 사용목적, 작용 원리, 생물학적 안전, 성능에 관한 자료는 품목 군에 따라 제출되는 범위와 큰 차이가 없습니다. 자세한 내용은 포스팅의 마지막에 첨부되는 첨부파일을 확인해 주세요.
3D 프린팅 의료기기의 가장 어려웠던 점은 바로 물리, 화학적 특성에 관한 자료입니다.
제출자료는 9가지가 있는데, 이 중 해당하지 않는다면 해당하지 않는다는 정당한 근거로 제조원의 선언서를 제출하면 됩니다.

1) 미세구조 분석 자료로 프린트된 표면을 확인할 수 있는 전자현미경 등의 사진을 제출할 수 있습니다.

2) 기공도 평가 자료로도 미세구조 분석 자료와 마찬가지로 전자현미경 등의 표면 사진으로 제출할 수 있습니다.

3) 표면 거칠기를 측정하여 제출하여야 합니다.

4) 표면 경도를 측정하여 제출하여야 합니다.

5) 밀도 평가 자료는 '금속 등을 이용한 3D 프린팅 제품'이라고 언급되어 있기 때문에 금속이 아니라면 제출 제외될 수 있습니다.

6) 치수 유효성 분석 자료는 실제 완성품의 치수를 측정하여 허용된 오차 범위 이내라는 성적서가 제출되면 됩니다.

7) 성분 분석 자료는 열, 레이저 등이 제품의 화학적 구조, 성분에 영향을 미치지 않는다는 것을 증명하기 위해 프린트되기 전의 재료와 프린트되어 경화된 재료의 성분분석 자료(예, EDX 등)가 필요합니다.

8) 생분해성 분석 자료는 인체에 이식, 삽입되는 의료기기의 경우 제출되어야 합니다.

9) 잔류물 분석 자료로 세척 밸리데이션 자료나 대한 약전에 의한 용출물 시험 보고서를 제출할 수 있습니다.
"3D 프린터를 이용하여 제조되는 맞춤형 의료기기 허가심사 가이드라인"에 저의 경험을 더해 작성해 봤는데, 혹시 틀린 내용이 있다면 알려주세요!