안녕하세요.
요즘 의료기기전자민원창구 웹사이트에서 팝업으로 의료기기 갱신제도가 계속 떠있어서 갱신제도에 대해 궁금한 사람들이 많은 것 같아요.
2020년 10월부터 갱신제도가 시행되어서 아직 갱신을 한 회사는 없을거라고 예상되지만 미리 준비하기 위해 정리를 해보겠습니다.

의료기기 갱신제도는 의료기기의 안전성과 유효성을 지속적으로 확보하기 위해 매 5년마다 품목허가, 신구를 주기적으로 갱신함으로써 체계적이고 실효적인 안전관리를 위해 만들어졌습니다.

이렇게 의료기기전자민원창구에서 팝업으로 뜨고있어서 많은 분들이 내용을 궁금해 하실것 같습니다.
2022년 의료기기 제조허가등 갱신에 관한 규정고시에 내용이 나와있지만 의료기기법, 시행규칙 등의 내용을 함께 봐야하기 때문에 주요내용만 정리해보았습니다.
1. 관련 규격
1) 의료기기 제조허가등 갱신에 관한 규정(제2022-1호)
2) 의료기기 허가 신고 심사 등에 관한 규정(제2022-52호)
3) 의료기기법(제18319호, 20220721)
4) 의료기기법 시행규칙(총리령 제1819호, 20220720)
5) 의료기기 제조허가등 갱신에 관한 규정 해설서(민원인안내서)(2021.10)
2. 갱신 신청서 제출 시기
유효기간이 끝나는 날의 180일 전까지
(180일전이 지나면 갱신신청 안됨. 무조건 180일 전까지 신청해야함.)
3. 시행규칙 제62조(유효기간 적용 제외 의료기기)
1) 수출만을 목적으로 하여 생산되거나 수입되는 수출용 의료기기
2) 법 제7조에 따라 조건부 제조허가 또는 제조인증을 받거나 조건부 제조신고를 한 의료기기(법 제15조제6항에서 준용하는 경우를 포함한다)
4. 법 제 49조의 6 : 갱신을 받을 수 없는 경우
제조업자 및 수입업자는 제1항에 따른 유효기간 동안 제조 또는 수입되지 아니한 의료기기에 대해서는 제3항에 따라 제조허가등을 갱신받을 수 없다. 다만, 총리령으로 정하는 부득이한 사유*로 제조 또는 수입되지 못한 의료기기의 경우에는 그러하지 아니하다
*시행규칙 제 62조의 2의 6
⑥ 법 제49조제6항 단서에서 “총리령으로 정하는 부득이한 사유”란 다음 각 호의 어느 하나에 해당하는 사유를 말한다. <개정 2022. 1. 21.>
1. 의료기기의 제조를 위한 원자재 공급이 이루어지지 않아 정상적인 제조 작업이 진행될 수 없었다고 인정되는 경우
2. 수출국가에서 의료기기 수출을 중단하거나 수출국가의 정치ㆍ경제적 상황으로 인해 정상적인 수입절차를 진행할 수 없었다고 인정되는 경우
3. 소수의 환자 등에 대해 적용되는 희소의료기기로서 해당 의료기기에 대한 수요가 없었다고 인정되는 경우
4. 그 밖에 제1호부터 제3호까지의 규정에 따른 사유와 유사한 것으로서 식품의약품안전처장이 정하여 고시하는 사유**
**의료기기 제조허가등 갱신에 관한 규정 제 4조의 3
③ 시행규칙 제62조의2제6항제4호에서 식약처장이 정하여 고시하는 사유란 다음 각 호를 말한다.
1. 갱신 대상 의료기기를 수리 또는 유지보수 하기 위해 필요한 부분품 또는 원자재를 제조ㆍ수입할 필요가 있다고 인정되는 경우
2. 생산ㆍ수입실적이 있는 특정 의료기기의 사용을 위해 특정 의료기기와 함께 사용하도록 제조허가등을 받은 갱신 대상 의료기기의 유효기간을 연장할 필요가 있다고 인정되는 경우
3. 시행규칙 제27조제1항제15호에 따라 의료기관으로부터 자기 회사가 제조한 의료기기를 구입한 경우로서 시행규칙 별표 2 제2호의 의료기기 제조 및 품질관리체계의 기준에 적합한지 검사한 실적이 있거나 시행규칙 제33조제1항제19호에 따라 의료기관으로부터 자기 회사가 수입한 의료기기를 구입한 경우로서 시행규칙 제33조제1항제7호다목의 시험규격에 적합한지 검사한 실적이 있는 경우
4. 시행규칙 제27조제1항제16호와 제33조제1항제20호에 따라 의료기기 판매업자 또는 임대업자로부터 시행규칙 제39조제1호가목에 따라 검사를 의뢰받은 의료기기로서 시행규칙 별표 2 제2호의 의료기기 제조 및 품질관리체계의 기준에 적합한지 검사한 실적이 있는 경우
5. 「의료법」제53조에 따라 갱신 대상 의료기기에 대한 신의료기술 평가가 진행 중이거나 신의료기술평가 결과 연구단계 의료기술로 통보를 받은 경우
5. 제출자료
|
순서
|
의료기기제조허가등갱신에 관한 규정
|
비고
|
|
1
|
해당 의료기기의 제조(수입) 허가증 또는 인증서 원본
|
|
|
2
|
이전 유효기간 동안 해당 의료기기의 안전성ㆍ유효성이 유지되고 있음을 증명하는 다음 각 목의 자료
|
-
|
|
|
가. 최신 규격의 반영 여부를 검토한 자료
|
고시 별지 제 2호 서식
|
|
|
나. 제품의 성능 및 안전성을 확인할 수 있는 자료로 체외진단의료기기를 제외한 의료기기는 허가규정 제26조제1항제4호에 해당하는 자료, 체외진단시약은 체진허가규정 제25조제1항제6호 및 제7호가목ㆍ다목ㆍ라목에 해당하는 자료, 체외진단장비는 체진허가규정 제25조제2항제4호가목부터 라목까지 해당하는 자료. 다만, 제조신고ㆍ수입신고 된 의료기기는 「의료기기 기준규격」(식품의약품안전처 고시)에 적합함을 입증하는 자료를 말한다.
|
성능, 유효기간, 생물시험성적서, 도면, MSDS등
|
|
3
|
이전 유효기간 동안 해당 의료기기의 생산 또는 수입 실적에 관한 자료
|
의료기기 생산,수입실적보고/의료기기 공급내역보고로 면제 가능
|
|
4
|
시행규칙 제62조의2제2항제4호에 따라 그 밖에 식약처장이 필요하다고 인정하는 자료로 다음 각 목에 해당하는 자료
|
갱신신청일 이후에 수집되는 자료는 제출 면제
|
|
|
가. 이전 유효기간 동안 수집된 안전성 정보 및 조치에 관한 자료
1) 시행규칙 제27조제1항제14호 및 제33조제1항제18호에 따른 시판 후 안전성ㆍ유효성과 관련된 정보 및 조치에 관한 자료 2) 1)에 따른 정보 및 조치에 관한 자료가 없는 경우에는 시행규칙 제27조제1항제4호 및 제33조제1항제3호에 따른 고객 불만처리 기록(이상사례 결과가 있는 경우에 한한다) 및 조치에 관한 자료와 시행규칙 별표 2 제2호나목11)호 시정 및 예방조치에 해당하는 자료(절차서ㆍ기준서 등 관련 문서) |
|
|
|
나. 시행규칙 제62조의2제6항 또는 이 규정 제4조제3항 각 호에 해당하는 경우에는 그 사유를 확인할 수 있는 자료
|
부득이한 사유로 제조 또는 수입되지 못한 의료기기의 경우
|
6. 허가 갱신 절차도
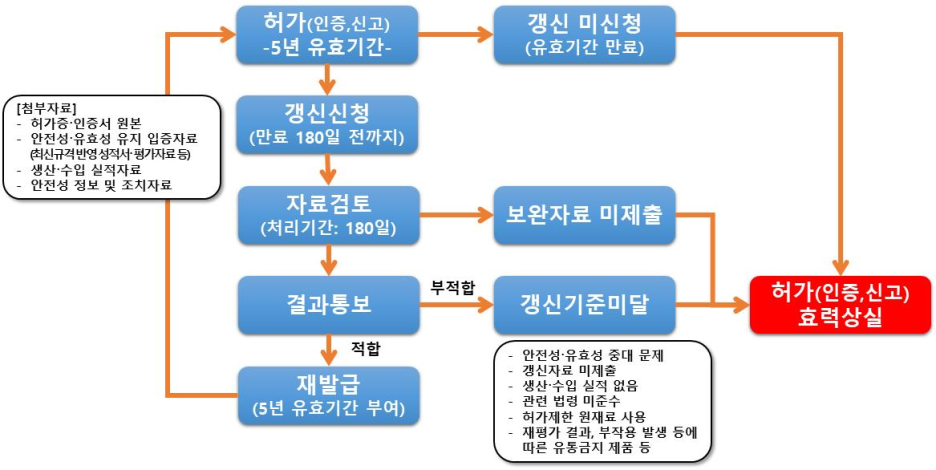
자세한 Q&A는 다음 포스팅에서 다뤄보겠습니다!
'의료기기 인허가RA' 카테고리의 다른 글
| 의료기기 해외/국외 비임상시험시험기관 (GLP) : OECD, FDA 인정기준 (0) | 2022.11.14 |
|---|---|
| 의료기기 제조/수입 품질책임자 자격요건, 제출서류 (0) | 2022.11.11 |
| 3D 프린트 맞춤형의료기기 인증,허가 주요내용 (0) | 2022.11.10 |
| 의료기기 비임상시험 실시기관 지정현황('22.7.15. 기준) (0) | 2022.11.08 |
| 의료기기 인허가/의료기기 ra 전문가 2급 자격증 정보 및 시험정보 (0) | 2022.11.07 |